搜索


近日,分子生物学知名刊物《Nucleic Acids Research》和病原微生物专业刊物《Virulence》先后发表了hbs红宝石平台、微生物代谢国家重点实验室邓子新团队欧竑宇研究组关于病原细菌耐药质粒播散的生物信息学分析工具和实验研究的两篇论文,进一步阐明以肺炎克雷伯菌为代表的ESKAPE耐药菌中耐药基因水平转移的分子机制。“oriTfinder: a web-based tool for the identification of origin of transfers in DNA sequences of bacterial mobile genetic elements”发表在《Nucleic Acids Research》上,李小彬为第一作者,欧竑宇为通讯作者。“Emergence of the third-generation cephalosporin-resistant hypervirulent Klebsiella pneumoniae due to the acquisition of a self-transferable blaDHA-1-carrying plasmid by an ST23 strain”发表在《Virulence》上,谢英洲、田李均和李刚为共同第一作者,欧竑宇和上海交大医学院附属瑞金医院重症学科刘嘉琳为共同通讯作者。
由于抗菌药物的不合理使用,病原细菌的耐药性日趋加剧。接合性质粒和整合性接合元件 (Integrative and conjugative element, ICE)具有接合转移位点oriT、松弛酶 (relaxase)、IV型伴侣蛋白 (type IV coupling proteins, T4CP) 和IV型分泌系统 (type IV secretion system, T4SS) 等四个转移功能模块,展现出滚环复制和接合转移等典型的单链DNA自行转移特性。获得性耐药基因常借助质粒和ICE等可移动遗传元件,通过接合转移等方式在细菌间水平转移。
为深度解读病原细菌的海量可移动基因组数据,欧竑宇研究组开发了生物信息学软件oriTfinder,用于快速识别质粒和ICE序列中的oriT、松弛酶、T4CP和T4SS等接合转移功能模块(图1)。首先,通过文本实体识别和语义提取,广泛地收集了散布于文献和公共数据库的异质数据,梳理了1千多个接合转移起始位点oriT的信息,定义和审编了nic位点附近保守序列,构建了可靠的训练集。其次,提出基于nic位点保守序列查找和邻近松弛酶基因共定位的新策略来识别质粒或ICE中的接合转移起始位点oriT;并基于oriT、松弛酶、T4CP和T4SS等4个功能区的不同预测结果,归类为接合转移、非自主转移和不可转移的质粒或ICE。oriTfinder在线工具的输入界面可支持细菌全基因组序列或未注释的contigs;输出界面可将oriT和T4SS等复杂的预测结果进行可视化显示。此外,oriTfinder还提供了Linux本地版,可用于细菌基因组序列的批量分析。
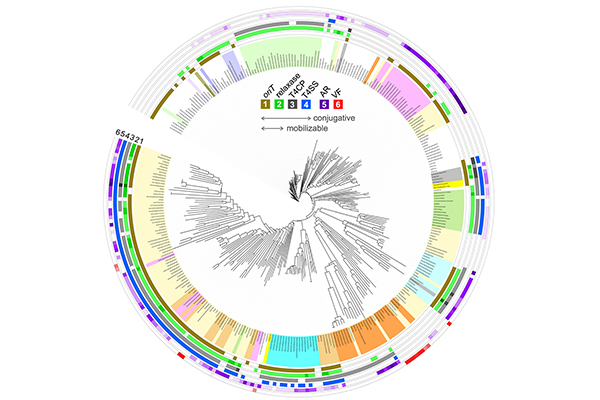
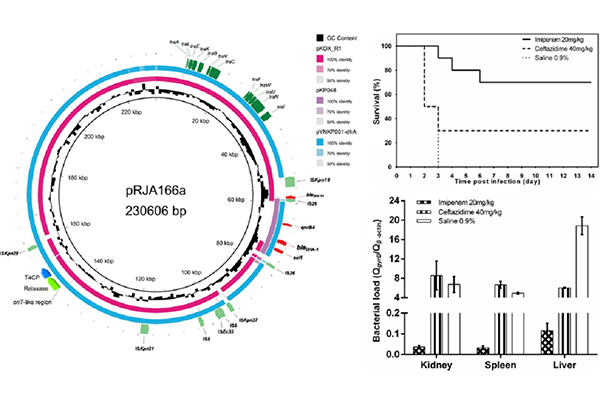
近年来,对于多重耐药高毒力肺炎克雷伯菌的报道呈现增多的趋势;但耐药质粒在高毒力肺炎克雷伯菌中的接合转移还未见报道。欧竑宇研究组在软件研发基础上,以在第三代头孢菌素耐药肺炎克雷伯菌为研究模型,开展耐药质粒接合转移的实验验证工作。研究人员和上海交通大学医学院附属瑞金医院重症学科瞿洪平教授研究组对分离自患者痰液样本的高耐药合并高毒力表型的肺炎克雷伯菌RJA166开展了合作研究(图2)。RJA166为ST23分型和K1荚膜表型,具有高黏液和高毒力表型 (拉丝实验阳性;BALB/c小鼠半数致死剂量为2.3×102 CFU);且对第三代头孢菌素具有耐药性 (头孢他啶MIC>64μg/ml);通过比较头孢他啶和亚胺培南对于RJA166感染小鼠的干预效果,确定了RJA166在小鼠体内同样具有对第三代头孢菌素的耐药性。RJA166有一个 230 kb的IncH耐药质粒pRJA166a,携带第三代头孢菌素抗性基因blaDHA-1。虽然在以大肠杆菌 HB101或J53作为pRJA166a接合转移实验的受体菌时,无法观察到接合子的出现;但根据oriTfinder软件的预测,pRJA166a是一个接合转移质粒,具有oriT、松弛酶、T4CP和T4SS等完整的转移功能区。研究人员进而尝试了其它受体菌,发现了pRJA166a具有从RJA166向肺炎克雷伯菌其他高毒株 (ST23型和ST374型) 和肺炎克雷伯菌碳青霉烯耐药株 (ST11 型) 发生接合转移的能力,转移频率约为 10-6/donor cell;而且,pRJA166a可在多种受体菌中稳定遗传,对受体菌毒力无显著影响。相关工作入选了2017年中国微生物学会学术年会的主旨报告和优秀学术交流奖。
邓子新团队的欧竑宇研究组长期从事肺炎克雷伯菌等耐药病原细菌的可移动基因组研究。以上两篇论文是继该研究组构建了细菌IV分泌系统数据库SecReT4 (Nucleic Acids Research, 2013)、开发了细菌ICE等可移动遗传元件识别软件VRprofile (Briefings in Bioinformatics, 2017)、发现了碳青霉烯酶基因blaKPC-2借助Tn1721-Tn3复合转座子在ST11型肺炎克雷伯菌中扩散 (Journal of Antimicrobial Chemotherapy,2015) 以来,取得的系统性进展。研究工作获得了国家自然科学基金和国家重点研发计划的资助。
论文链接:
https://academic.oup.com/nar/article/46/W1/W229/4992657
https://www.tandfonline.com/doi/full/10.1080/21505594.2018.1456229
文字 | 欧竑宇


 首页
首页

 学院概况
学院概况

 师资队伍
师资队伍

 人才培养
人才培养

 招生就业
招生就业

 科学研究
科学研究

 平台基地
平台基地

 党群工作
党群工作

 校友之家
校友之家

 安全工作
安全工作

 网上办事
网上办事

 当前位置:
当前位置: